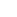Servizi CDMO per vettori lentivirali - IIT Grade/non - Fase clinica
Servizi
| Servizi CDMO per vettori lentivirali (piattaforma Hilenti®) | ||||
| Tipi | Servizi | |||
|
Grado iIT |
1 | Sistema di quattro - plasmidi sviluppato in modo indipendente |
● Terza generazione Four - Sistema plasmide ● Kanamicina - Gene di resistenza ● Nessuna licenza di brevetto richiesta |
● Connessione senza soluzione di continuità alla presentazione IND |
| 2 | Produzione e test di vettori lentivirali (GMP - come) |
● Output di produzione adattabile e specifiche |
● GMP - Like Workshop ● Documentazione autentica e tracciabile ● GMP - Sistema di gestione della qualità |
|
Vantaggi
| Vantaggi dell'utilizzo della nostra piattaforma per il siero - Cultura di sospensioni gratuite di vettori lentivirali:
• privo di animali da animale - derivati durante tutto il processo • produzione linearmente ridimensionata di vettori lentivirali • Utilizzo di un singolo contenitore di un bioreattore usa e getta da 50 L • Creazione della banca cellulare in seminari separati • Distribuzione di prodotti finali utilizzando un isolatore sterile • Sistema lentivirus dedicato per cellule CAR - T, con alta efficienza di infezione • Bassi costi di produzione e costi di test (nessun requisito di test per BSA e enzimi pancreatici residui) • Diverse comunicazioni INS di successo all'NMPA dei vettori lentivirali per le cellule CAR - T |
Processo di produzione
Controllo di qualità
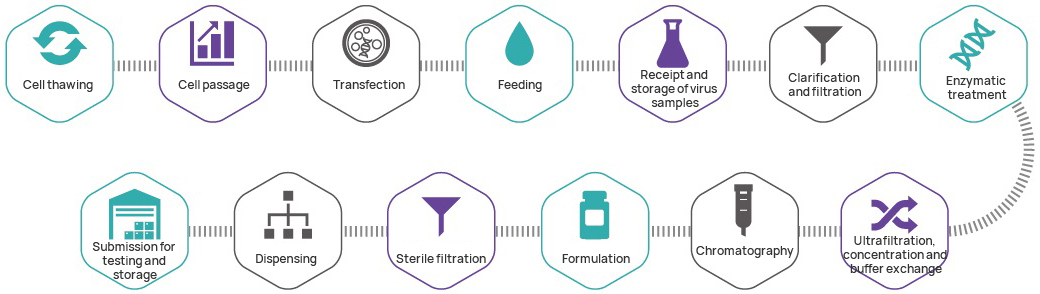
| Prodotto | Articolo di prova | Metodo di prova |
| Raccolta fluido | Contaminazione da virus avventizie | Metodo 3302 di CHP 2020 |
| Replica - lentivirus competenti | Metodo di coltura cellulare indicatore | |
| Sostanza farmacologica/prodotto finito | Aspetto | Ispezione visiva |
| Sterilità | Metodo 1101 di CHP 2020 | |
| Micoplasma |
Metodo 3301 di CHP 2020 |
|
| pH | Metodo 0631 di CHP 2020 | |
| Osmolalità | Metodo 0632 di CHP 2020 | |
| Identificazione della struttura genica bersaglio | Sequenziamento | |
| Proteina residua di cellule ospiti | Elisa | |
| Titolo fisico (P24) | Elisa | |
| Titolo funzionale | Citometria a flusso | |
| Endotossina | Metodo 1143 di CHP 2020 | |
| Benzonasi residua | Elisa | |
| DNA residuo di cellule ospiti | Q - PCR | |
| Trasferimento genico residuo E1A | Metodo CO - Cultura | |
| Trasferimento genico residuo SV40 | Metodo CO - Cultura |
Cronologia del progetto
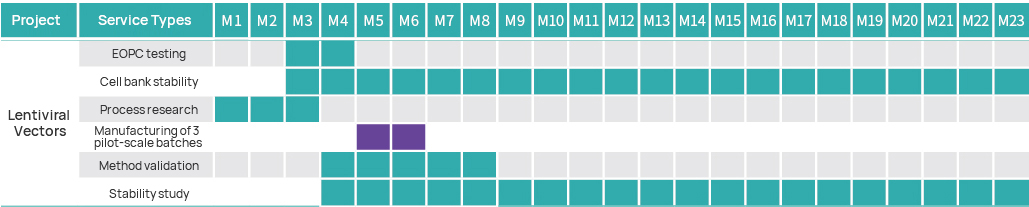
Piano di gestione del progetto
Hillgene Project Management Team, composto da scienziati principali, project manager, esperti di progetto QA e GMP, farà sforzi per garantire il funzionamento regolare e solido di ogni progetto GMP.