Dịch vụ CDMO cho vectơ lentivirus - Lớp Ind
Dịch vụ
| Lớp Ind | 1 | Phát triển độc lập bốn hệ thống - plasmid |
● Bốn thế hệ thứ ba - Hệ thống plasmid ● Kanamycin - gen kháng ● cấp giấy phép, nếu được yêu cầu |
● Các tiêu chuẩn sau đây để nộp tại cả Trung Quốc và Hoa Kỳ ● Toàn bộ - Hội thảo GMP ● Khu vực riêng biệt để tạo ngân hàng di động ● Các hội thảo riêng biệt trong các khu vực không vô trùng và vô trùng ● Hệ thống quản lý chất lượng GMP |
| 2 | Tạo ra ngân hàng di động GMP |
● Số lượng ngân hàng di động được tạo ra ● Nghiên cứu ổn định của ngân hàng di động |
||
| 3 | Phát triển phương pháp xử lý và thử nghiệm |
● Yêu cầu dự án sau (tùy thuộc vào các thay đổi tùy chỉnh) |
||
| 4 | GMP sản xuất vectơ lentivirus |
● Quá trình sinh học: 5 ~ 50 L Quy trình sinh học dùng một lần (tùy thuộc vào các thay đổi tùy chỉnh) ● Thang đo sản xuất: 2 ~ 30 L (tùy theo thay đổi tùy chỉnh) |
||
| 5 | Thử nghiệm các vectơ lentivirus |
● Chuẩn độ vật lý ● Chuẩn độ nhiễm trùng ● Chuẩn độ chức năng ● Xét nghiệm DNA tế bào chủ 293T còn lại ● Xét nghiệm protein tế bào chủ còn lại 293T ● Xét nghiệm DNA ngoại sinh còn lại ● Thử nghiệm benzonase còn lại ● E1A/SV40 ● Kiểm tra plasmid còn lại ● Kích thước mảnh DNA ● Virokine ngoại sinh ● Vô số ● Mycoplasma ● Endotoxin |
||
| 6 | Xác thực phương pháp |
● Tính đặc hiệu ● Độ chính xác ● Độ chính xác ● Độ tuyến tính và phạm vi ● LOD |
||
| 7 | Nghiên cứu ổn định |
● Long - độ ổn định thời hạn ● Tính ổn định tăng tốc ● Kiểm tra căng thẳng |
Thuận lợi
| Ưu điểm của việc sử dụng nền tảng của chúng tôi cho huyết thanh - Nuôi cấy hệ thống treo miễn phí của vectơ lentivirus:
• Không có động vật - Các thành phần có nguồn gốc trong suốt quá trình • Sản xuất mở rộng tuyến tính của vectơ lentivirus • Sử dụng một thùng chứa chất phản ứng sinh học dùng một lần 50 L • Tạo ngân hàng di động trong các hội thảo riêng biệt • Phân phối các sản phẩm cuối cùng bằng cách sử dụng bộ phân lập vô trùng • Hệ thống lentirus chuyên dụng cho các tế bào xe hơi, với hiệu quả nhiễm trùng cao • Chi phí sản xuất thấp và chi phí thử nghiệm (không có yêu cầu thử nghiệm cho BSA và enzyme tụy còn lại) • Một số bài nộp IND thành công đến NMPA của vectơ lentivirus cho các tế bào xe hơi |
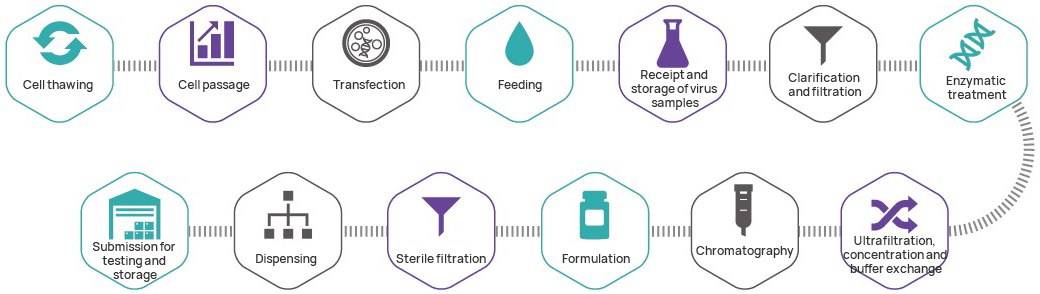
Quá trình sản xuất
Kiểm soát chất lượng
| Sản phẩm | Mục kiểm tra | Phương pháp kiểm tra |
| Thu hoạch chất lỏng | Ô nhiễm virus phiêu lưu | Phương pháp 3302 của CHP 2020 |
| Sao chép - Lentivirus có thẩm quyền | Phương pháp nuôi cấy tế bào chỉ báo | |
| Chất thuốc/thành phẩm | Vẻ bề ngoài | Kiểm tra trực quan |
| Vô sinh | Phương pháp 1101 của CHP 2020 | |
| Mycoplasma |
Phương pháp 3301 của CHP 2020 |
|
| pH | Phương pháp 0631 của CHP 2020 | |
| Sự thẩm thấu | Phương pháp 0632 của CHP 2020 | |
| Nhận dạng cấu trúc gen mục tiêu | Trình tự | |
| Protein tế bào chủ còn lại | ELISA | |
| Chuẩn độ vật lý (p24) | ELISA | |
| Chuẩn độ chức năng | Dòng tế bào học | |
| Nội độc tố | Phương pháp 1143 của CHP 2020 | |
| Benzonase còn lại | ELISA | |
| DNA tế bào chủ còn lại | Q - PCR | |
| Chuyển gen E1A dư | CO - Phương pháp văn hóa | |
| Chuyển gen sv40 còn lại | CO - Phương pháp văn hóa |
Dòng thời gian dự án
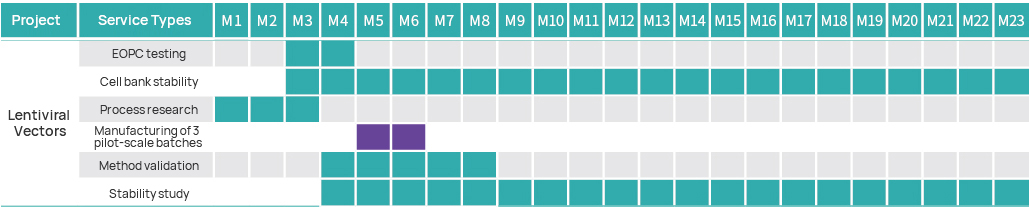
Kế hoạch quản lý dự án
Đội ngũ quản lý dự án Hillgene, bao gồm các nhà khoa học trưởng, quản lý dự án, các chuyên gia dự án QA và GMP, sẽ nỗ lực để đảm bảo hoạt động trơn tru và hợp lý của mỗi dự án GMP.