CDMO -tjänster för plasmider - Ind -klass
Tjänster
| CDMO -tjänster för plasmider | ||||
| Typ | Tjänster | |||
| Ind -klass | 1 | Oberoende utvecklade fyra - plasmidsystem |
● Tredje generationens fyra - Plasmidsystem ● Kanamycin - resistensgen ● Bevilja licensen, vid behov |
● Följer standarder för inlämning i både Kina och USA ● Full - GMP -workshop ● Separat område för att skapa cellbanker ● Separata workshops inom icke -sterila och sterila områden ● GMP -kvalitetshanteringssystem |
| 2 | GMP skapande av bakteriecellbank |
● Val av monoklonala antikroppar ● Skräddarsydd antal cellbanker som ska skapas ● Cell Bank Stability Study |
||
| 3 | Process- och testmetodutveckling |
● Efter projektkrav (med förbehåll för anpassade förändringar) |
||
| 4 | GMP -tillverkning av plasmider |
● Produktionsproduktion: 10 mg ~ 1 g (med förbehåll för anpassade förändringar) ● Fermenteringsvolym: 3 ~ 30 L (med förbehåll för anpassade ändringar) ● Reningsmetod: Tre - Stegmetod/två - Stegmetod |
||
| 5 | Plasmidtestning |
● Renhet (HPLC) ● Rest E.Coli DNA -testning ● Rest E.Coli HCP -testning ● Rest E.Coli RNA -testning ● Resterande antibiotikatestning ● Sterilitet ● Mycoplasma ● Endotoxin |
||
| 6 | Metodvalidering |
● Specificitet ● Noggrannhet ● Precision ● Linearitet och räckvidd ● LOD |
||
| 7 | Stabilitetsstudie |
● Lång - Term stabilitet ● Accelererad stabilitet ● Stresstestning |
||
Fördelar
| Fördelar med vårt plasmidsystem:
• Ett oberoende utvecklat fyra - plasmidsystem med kanamycin - resistensgen • Ett system med kapacitet för långvarig optimering • Plasmidsekvenser är spårbara, överensstämmer med kraven och effektiva • Omfattande erfarenhet av framgångsrika Ind -inlämningar • CAR - T -cellprover för klinisk användning tillverkas och används för närvarande • 2 - 5 veck högre titrar efter att ha använt vårt plasmidsystem från jämförelsen i flera projekt |
Fördelar med vår plasmidtillverkning: • fri från antibiotika under tillverkningsprocessen • Plasmidproduktion och bankskapande i separata workshops • Fullständig isolering mellan icke -sterila och sterila områden • Dispensering av slutprodukter med en isolator • Avslutad CTD -dossiers för förpackningsplasmid (för lentiviral vektor), vilket minskar inlämningsberedningstiden med 3 - 4 månader, med Inds av några få produkter som beviljats preliminärt godkännande och för närvarande i fas I i klinisk studie |
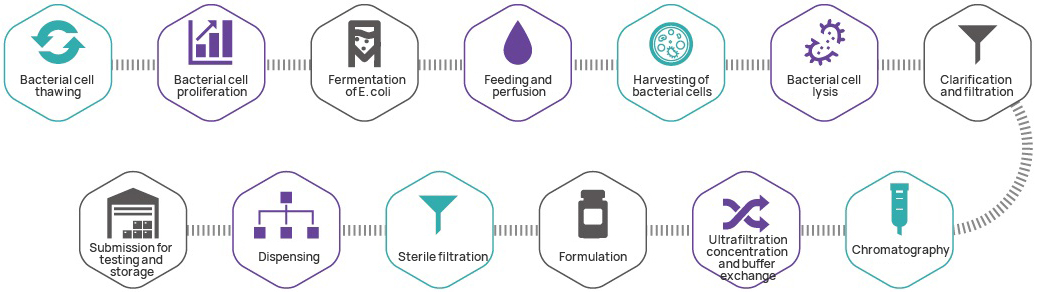
Tillverkningsprocess
Kvalitetskontroll
| Testobjekt | Testmetod | |
| Utseende | Visuell inspektion | |
| Identifiering | Identifiering 1 | Restriktionskartläggning |
| Identifiering 2 | Sanger sekvensering | |
| Testa | pH | Metod 0631 av CHP 2020 |
| Renhet | High Performance Liquid Chromatography (HPLC) | |
| Rest E.Coli värdcellprotein | Elisa | |
| Rest E.coli DNA | Q - PCR | |
| Rest E.coli RNA | Q - PCR | |
|
Resterande antibiotika |
Elisa | |
| Endotoxin | Metod 1143 i CHP 2020 | |
| Sterilitet | Metod 1101 i CHP 2020 | |
| Koncentrationsbestämning | DNA -koncentration | Metod 0401 av CHP 2020 |
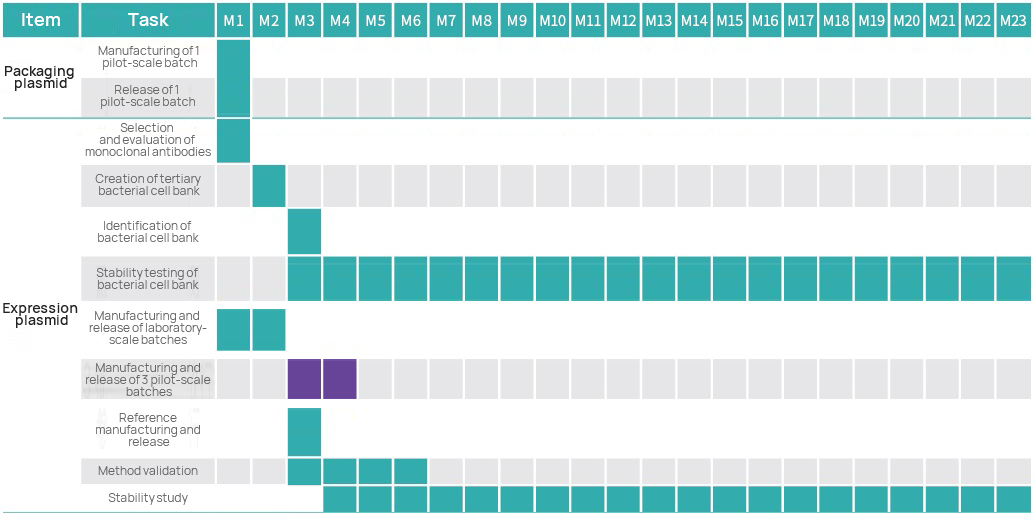
Projekttidslinje
Projektledningsplan
Hillgene Project Management Team, bestående av chefsforskare, projektledare, projekt QA- och GMP -experter, kommer att göra ansträngningar för att säkerställa en smidig och sund drift av varje GMP -projekt.