Služby CDMO pre plazmidy - IND GRADE
Služby
| Služby CDMO pre plazmidy | ||||
| Typy | Služby | |||
| IND známka | 1 | Nezávisle vyvinutý štyri - plazmidový systém |
● Systém tretej generácie Four - Plazmidový systém ● Kanamycín - rezistenčný gén ● V prípade potreby udelenie licencie |
● Nasledujúce normy podriadenia sa v Číne aj v USA ● Úplný workshop GMP ● Samostatná oblasť na vytváranie mobilných bánk ● Samostatné workshopy v ne - Sterilných a sterilných oblastiach ● Systém riadenia kvality GMP |
| 2 | GMP vytváranie bakteriálnej bunkovej banky |
● Výber monoklonálnych protilátok ● Prispôsobiteľný počet bunkových bánk, ktoré sa majú vytvoriť ● Štúdia stability buniek |
||
| 3 | Vývoj metódy procesu a testovania |
● Podľa požiadaviek projektu (s výhradou prispôsobených zmien) |
||
| 4 | Výroba plazmidov GMP |
● Výstupný výstup: 10 mg ~ 1 g (s výhradou prispôsobených zmien) ● Objem fermentácie: 3 ~ 30 l (s výhradou prispôsobených zmien) ● Metóda čistenia: Tri - Krokový prístup/Two - Krokový prístup |
||
| 5 | Testovanie plazmidov |
● Čistota (HPLC) ● Zvyšné testovanie DNA E.coli ● Zvyšné testovanie E.Coli HCP ● Zvyšné testovanie E.coli RNA ● Testovanie zvyškových antibiotík ● Sterilita ● Mycoplasma ● endotoxín |
||
| 6 | Overenie metódy |
● špecifickosť ● Presnosť ● Presnosť ● Linearita a rozsah ● LOD |
||
| 7 | Štúdium stability |
● Dlhá - termínová stabilita ● Zrýchlená stabilita ● Testovanie napätia |
||
Výhody
| Výhody nášho plazmidového systému:
• nezávisle vyvinutý štyri - plazmidový systém s kanamycínom - rezistenčný gén • Systém so schopnosťou trvalej optimalizácie • Plazmidové sekvencie sú sledovateľné, sú v súlade s požiadavkami a efektívne • Rozsiahle skúsenosti s úspešnými podaniami IND • Vzorky automobilu - T buniek na klinické použitie sa v súčasnosti vyrábajú a používajú • 2 - 5 záhyby vyšších titrov po použití nášho plazmidového systému z porovnania v niekoľkých projektoch |
Výhody našej výroby plazmidov: • Bez antibiotík počas celého výrobného procesu • Výroba plazmidov a tvorba bánk v samostatných seminároch • Kompletná izolácia medzi ne - sterilnými a sterilnými oblasťami • Dávku konečných výrobkov pomocou izolátora • Dokončené CTD dokumentácie pre balenie plazmidu (pre lentivírusový vektor), čím sa skráti čas prípravy predloženia o 3 - 4 mesiace, pričom IND z niekoľkých výrobkov udelilo predbežné schválenie av súčasnosti vo fáze I klinickej štúdie |
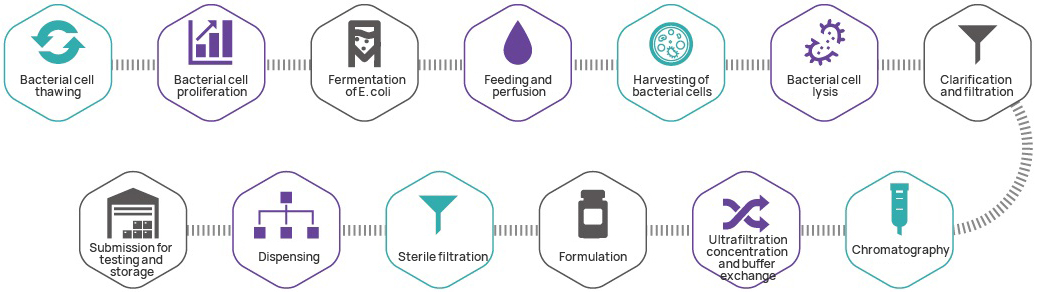
Výrobný proces
Kontrola kvality
| Skúšobná položka | Skúšobná metóda | |
| Vzhľad | Vizuálna kontrola | |
| Identifikácia | Identifikácia 1 | Mapovanie obmedzenia |
| Identifikácia 2 | Sekvenovanie Sanger | |
| Skúška | pH | Metóda 0631 z CHP 2020 |
| Čistota | Vysokoúčinná kvapalná chromatografia (HPLC) | |
| Zvyškový proteín hostiteľských buniek E.coli | Elisa | |
| Zvyšková DNA E.COLI | Q - PCR | |
| Zvyšková E.Coli RNA | Q - PCR | |
|
Zvyškové antibiotiká |
Elisa | |
| Endotoxín | Metóda 1143 CHP 2020 | |
| Sterilita | Metóda 1101 z CHP 2020 | |
| Stanovenie koncentrácie | Koncentrácia DNA | Metóda 0401 z CHP 2020 |
Časová os projektu
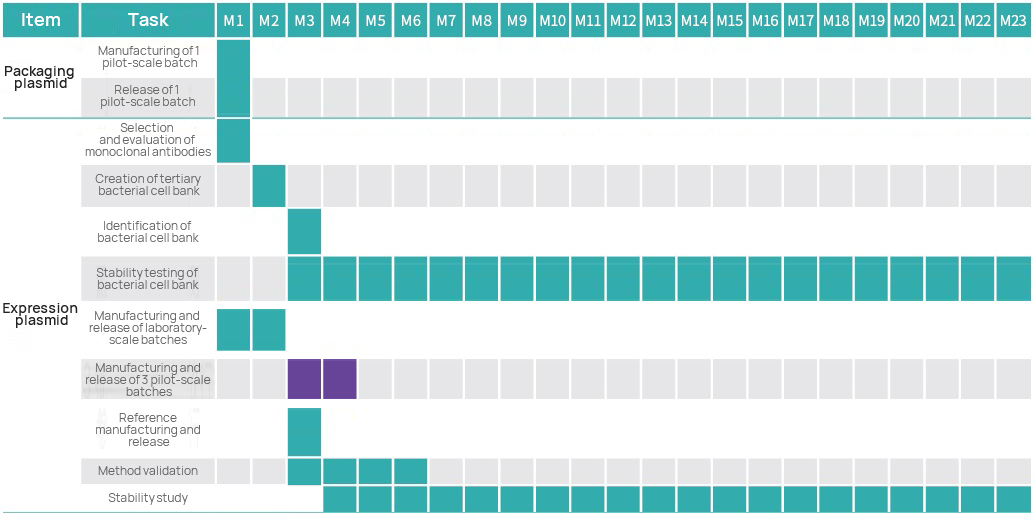
Plán riadenia projektu
Tím Hillgene Project Management, ktorý sa skladá z hlavných vedcov, projektových manažérov, odborníkov na projekt QA a GMP, vyvinie úsilie na zabezpečenie hladkej a zvukovej prevádzky každého projektu GMP.