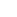Necesitatea testării ADN -ului rezidual E.coli
În câmpuri precum terapia cu celule și gene, plasmidele virale sunt amplificate și fermentate folosind E. coli ca gazdă. Plasmida amplificată trebuie să fie supusă controlului calității ADN -ului rezidual E.coli înainte de a putea fi utilizat pentru a infecta 293 de celule și pentru a împacheta virusul. Prin urmare, detectarea ADN -ului rezidual E.coli este critică.
Cerințe de reglementare și metode de testare
Ghidurile actuale OMS și FDA din SUA recomandă ADN -ului rezidual în produsele finite să nu fie mai mare de 10 ng/agent, iar FDA din SUA afirmă, de asemenea, că ADN -ul rezidual în celulele gazdă ale biologicelor nu ar trebui să fie mai mare de 100 pg/agent. Principiile generale ale farmacopeei europene prevede că limita ADN -ului rezidual în produsele biologice nu ar trebui să fie mai mare de 10 ng/doză, dar limita de ADN reziduală pentru anumite vaccinuri este mai strictă, de exemplu, ADN -ul rezidual în vaccinul inactivat împotriva hepatitei A nu ar trebui să fie mai mare de 100 pg/doză și că vaccinul împotriva Hepatitei B, nu ar trebui să fie mai mare de 10 PG/doză. Ediția din 2020 a farmacopeei chineze, partea a III -a, prevede că reziduul de ADN în preparatele biologice produse pe o matrice celulară nu trebuie să depășească 100 pg/doză, iar reziduul de ADN în vaccinurile produse pe o matrice bacteriană sau fungică nu trebuie să depășească 10 Ng/doză.
În plus, pentru metodele de determinare a reziduurilor de ADN exogene, farmacopeele naționale oferă, de asemenea, recomandări de orientare. Ediția Farmacopeiei din SUA 2017 a USP40 - NF35 Dispoziția generală 1130 descrie trei metode pentru determinarea reziduurilor de ADN exogene, care sunt hibridizarea sondei ADN, metoda pragului și metoda PCR cantitativă reală - Farmacopeea europeană propune PCR cantitativ în timp real și metoda imunoenzimatică, două metode analitice sensibile pentru cuantificarea ADN -ului rezidual cu celule gazdă. Versiunea de farmacopeie chineză 2020 a celor trei reguli generale 3407 prevede, de asemenea, că metodele de detectare a reziduurilor ADN -ului celulelor gazdă sunt hibridizarea sondei ADN, colorarea fluorescenței și PCR cantitativă.
Printre aceștia, metoda qPCR are o sensibilitate extrem de ridicată, specificitatea secvenței și precizia, ceea ce poate oferi un mijloc de detectare fiabil pentru industria biofarmaceutică în cercetarea procesului și controlul calității produselor finite, iar acum a devenit metoda preferată de detectare pentru fiecare producător biologic.
Informații despre produsele Bluekit
Caracteristici ale produsului
Detectarea rapidă, specificitate puternică, performanță fiabilă, cea mai mică limită de detecție poate atinge nivelul „FG”.
Parametrii produsului
- Interval de detectare: 3.00 × 101 ~ 3.00 × 105fg/µl
- Limita cuantificării :00 × 101fg/µl
- Limita de detectare :00 FG/µL
- Precizie: CV% ≤ 15%.
Probleme comune de detectare și precauții
1. Acest kit este doar pentru utilizarea cercetării in vitro, nu pentru diagnosticul clinic.
2. Kitul trebuie utilizat în perioada de validitate.
3. Toate componentele din kit sunt recomandate să fie topite într -un mediu scăzut de temperatură și apoi utilizate.
4. Doar respectă cu strictețe instrucțiunile metodei de funcționare, toată utilizarea kitului de susținere a reactivilor pentru a asigura cel mai bun efect de detectare.
5. Acordați atenție diferitelor etape de eșantionare în timp util pentru a înlocui vârful, pentru a evita contaminarea încrucișată, evitați deschiderea capacului mult timp.
6. Rezultatele finale ale testelor pot fi afectate semnificativ de eficacitatea reactivilor, de metodele de operare ale operatorului și de mediul de testare.
Consultarea produsului
Telefon: +86 - 18013115357
E-mail:info@hillgene.com
Ora post: 2024 - 01 - 11 10:31:30