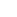CDMO -services voor plasmiden - Ind -graad
Diensten
| CDMO -services voor plasmiden | ||||
| Soorten | Diensten | |||
| Ind -graad | 1 | Onafhankelijk ontwikkeld vier - plasmidesysteem |
● Derde generatie vier - Plasmidesysteem ● Kanamycin - resistentiegen ● De licentie verlenen, indien nodig |
● Volg de normen voor indiening in zowel China als de VS ● Volledige - GMP -workshop ● Afzonderlijk gebied voor het maken van celbanken ● afzonderlijke workshops binnen niet -- steriele en steriele gebieden ● GMP Quality Management System |
| 2 | GMP Creation of Bacterial Cell Bank |
● Selectie van monoklonale antilichamen ● Tailerable aantal te maken celbanken ● Studie voor stabiliteit van de celbank |
||
| 3 | Ontwikkeling van proces- en testmethode |
● Na projectvereisten (afhankelijk van aangepaste wijzigingen) |
||
| 4 | GMP -productie van plasmiden |
● Productie -output: 10 mg ~ 1 g (onder voorbehoud van aangepaste wijzigingen) ● Fermentatievolume: 3 ~ 30 L (onder voorbehoud van aangepaste wijzigingen) ● Zuiveringsmethode: drie - Stapbenadering/twee - Stapbenadering |
||
| 5 | Plasmide -testen |
● Zuiverheid (HPLC) ● Residuele e.coli -DNA -testen ● Residuele e.coli HCP -testen ● Residuele e.coli RNA -testen ● Residuele antibiotica -testen ● Steriliteit ● Mycoplasma ● Endotoxine |
||
| 6 | Methode validatie |
● specificiteit ● Nauwkeurigheid ● Precisie ● Lineariteit en bereik ● LOD |
||
| 7 | Stabiliteitsstudie |
● Lang - Termijnstabiliteit ● Versnelde stabiliteit ● Stresstests |
||
Voordelen
| Voordelen van ons plasmidesysteem:
• Een onafhankelijk ontwikkeld vier - plasmide -systeem met kanamycine - resistenti • Een systeem met de mogelijkheid van aanhoudende optimalisatie • Plasmide -sequenties zijn traceerbaar, voldoen aan de vereisten en efficiënt • Uitgebreide ervaring in succesvolle IND -inzendingen • Auto - T -celmonsters voor klinisch gebruik zijn momenteel productie en in gebruik • 2 - 5 vouwen hogere titers na het gebruik van ons plasmide -systeem uit de vergelijking in verschillende projecten |
Voordelen van onze plasmide -productie: • Vrij van antibiotica gedurende het productieproces • Plasmide -productie en het maken van bankbanken in afzonderlijke workshops • Volledige isolatie tussen niet -- steriele en steriele gebieden • Afgifte van eindproducten met behulp van een isolator • Voltooide CTD -dossiers voor verpakkingsplasmide (voor lentivirale vector), waardoor de inzendingstijd met 3 - 4 maanden wordt verkort, met Inds van een paar producten die voorlopige goedkeuring hebben verleend en momenteel in fase I van klinische studie |
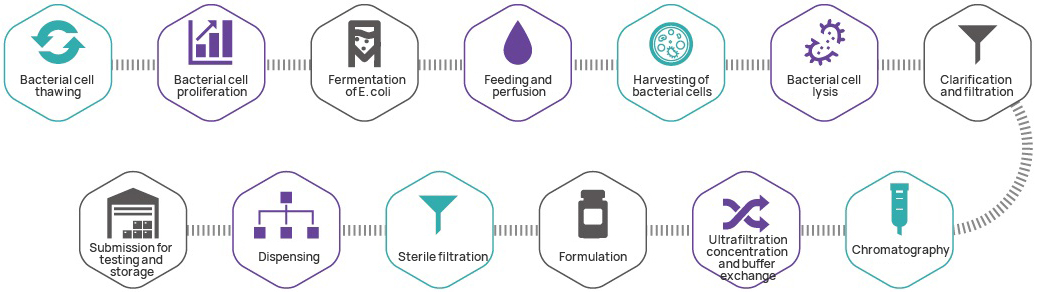
Productieproces
Kwaliteitscontrole
| Testitem | Testmethode | |
| Verschijning | Visuele inspectie | |
| Identificatie | Identificatie 1 | Beperking Mapping |
| Identificatie 2 | Sanger -sequencing | |
| Test | pH | Methode 0631 van CHP 2020 |
| Zuiverheid | High Performance Liquid Chromatography (HPLC) | |
| Resterende e.coli -gastheercel -eiwit | ELISA | |
| Residueel e.coli -DNA | Q - PCR | |
| Residueel e.coli RNA | Q - PCR | |
|
Resterende antibiotica |
ELISA | |
| Endotoxine | Methode 1143 van CHP 2020 | |
| Steriliteit | Methode 1101 van CHP 2020 | |
| Concentratiebepaling | DNA -concentratie | Methode 0401 van CHP 2020 |
Projecttijdlijn
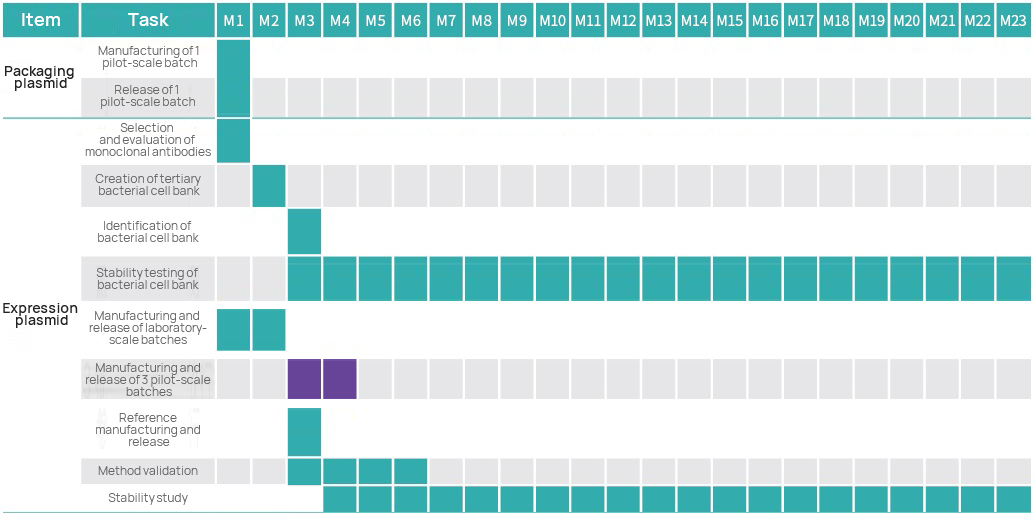
Projectmanagementplan
Hillgene Project Management Team, bestaande uit hoofdwetenschappers, projectmanagers, Project QA en GMP -experts, zal inspanningen leveren om de soepele en degelijke werking van elk GMP -project te waarborgen.