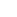CDMO -services voor lentivirale vectoren - Ind -graad
Diensten
| Ind -graad | 1 | Onafhankelijk ontwikkeld vier - plasmidesysteem |
● Derde generatie vier - Plasmidesysteem ● Kanamycin - resistentiegen ● De licentie verlenen, indien nodig |
● Volg de normen voor indiening in zowel China als de VS ● Volledige - GMP -workshop ● Afzonderlijk gebied voor het maken van celbanken ● afzonderlijke workshops binnen niet -- steriele en steriele gebieden ● GMP Quality Management System |
| 2 | Creatie van GMP Cell Bank |
● Tailerable aantal te maken celbanken ● Studie voor stabiliteit van de celbank |
||
| 3 | Ontwikkeling van proces- en testmethode |
● Na projectvereisten (afhankelijk van aangepaste wijzigingen) |
||
| 4 | GMP -productie van lentivirale vectoren |
● Bioreactor -proces: 5 ~ 50 L wegwerpbaar bioreactorproces (onder voorbehoud van aangepaste wijzigingen) ● Productieschaal: 2 ~ 30 L (onder voorbehoud van aangepaste wijzigingen) |
||
| 5 | Testen van lentivirale vectoren |
● Fysieke titer ● Infectieve titer ● Functionele titer ● Residuele 293T hostcel -DNA -testen ● Residuele 293T -test van gastheercellen ● Residuele exogene DNA -testen ● Residuele benzonasetesten ● E1A/SV40 ● Residuele plasmide -testen ● DNA -fragmentgrootte ● Exogene Virokines ● Steriliteit ● Mycoplasma ● Endotoxine |
||
| 6 | Methode validatie |
● specificiteit ● Nauwkeurigheid ● Precisie ● Lineariteit en bereik ● LOD |
||
| 7 | Stabiliteitsstudie |
● Lang - Termijnstabiliteit ● Versnelde stabiliteit ● Stresstests |
Voordelen
| Voordelen van het gebruik van ons platform voor serum - Gratis ophanging van lentivirale vectoren:
• Vrij van dier - afgeleide componenten gedurende het hele proces • Lineair opgeschaalde productie van lentivirale vectoren • Met behulp van een enkele container van een wegwerpbare bioreactor van 50 l • Celbankcreatie in afzonderlijke workshops • Afgifte van eindproducten met behulp van een steriele isolator • Dedicated Lentivirus -systeem voor auto - T -cellen, met een hoge infectie -efficiëntie • Lage productiekosten en testkosten (geen testen vereisten voor BSA en resterende pancreasenzymen) • Verschillende succesvolle IND -inzendingen aan NMPA van lentivirale vectoren voor auto - T -cellen |
Productieproces
Kwaliteitscontrole
| Product | Testitem | Testmethode |
| Oogstvloeistof | Adventieve virusverontreiniging | Methode 3302 van CHP 2020 |
| Replicatie - Competente lentivirussen | Indicatorcelkweekmethode | |
| Drugsubstantie/eindproduct | Verschijning | Visuele inspectie |
| Steriliteit | Methode 1101 van CHP 2020 | |
| Mycoplasma |
Methode 3301 van CHP 2020 |
|
| pH | Methode 0631 van CHP 2020 | |
| Osmolaliteit | Methode 0632 van CHP 2020 | |
| Identificatie van doelgenstructuur | Volgorde | |
| Resterende gastheercel -eiwit | ELISA | |
| Fysieke titer (P24) | ELISA | |
| Functionele titer | Flowcytometrie | |
| Endotoxine | Methode 1143 van CHP 2020 | |
| Resterende benzonase | ELISA | |
| Resterende gastheercel -DNA | Q - PCR | |
| Resterende E1A -genoverdracht | CO - Cultuurmethode | |
| Resterende SV40 -genoverdracht | CO - Cultuurmethode |
Projecttijdlijn
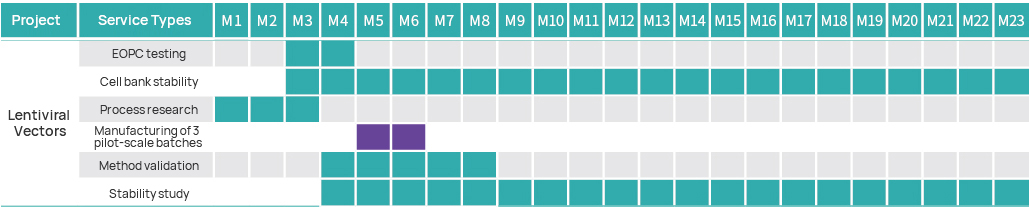
Projectmanagementplan
Hillgene Project Management Team, bestaande uit hoofdwetenschappers, projectmanagers, Project QA en GMP -experts, zal inspanningen leveren om de soepele en degelijke werking van elk GMP -project te waarborgen.