CDMO pakalpojumi plazmīdām - Ind pakāpe
Pakalpojumi
| CDMO pakalpojumi plazmīdām | ||||
| Veidi | Pakalpojumi | |||
| IND pakāpe | 1 | Patstāvīgi izstrādāta četras - plazmīdu sistēma |
● Trešās paaudzes četras paaudzes - plazmīdu sistēma ● Kanamicīns - rezistences gēns ● Ja nepieciešams licences piešķiršana |
● Pēc iesniegšanas standartiem gan Ķīnā, gan ASV ● Pilns - GMP darbnīca ● Atsevišķa zona šūnu banku izveidošanai ● Atsevišķas darbnīcas, kas nav - sterilās un sterilās zonās ● GMP kvalitātes pārvaldības sistēma |
| 2 | GMP baktēriju šūnu bankas izveidošana |
● Monoklonālo antivielu izvēle ● Atbalstāms šūnu banku skaits, kas jāizveido ● Šūnu bankas stabilitātes pētījums |
||
| 3 | Procesa un testa metodes izstrāde |
● Pēc projekta prasībām (uz tiem pielāgotām izmaiņām) |
||
| 4 | GMP plazmīdu ražošana |
● Ražošanas izvade: 10 mg ~ 1 g (piemērotas izmaiņas) ● Fermentācijas tilpums: 3 ~ 30 L (uz tiem pielāgotām izmaiņām) ● Attīrīšanas metode: trīs - STEP pieeja/Divas - STEP pieeja |
||
| 5 | Plazmīdu pārbaude |
● tīrība (HPLC) ● Atlikušā E.Coli DNS pārbaude ● Atlikušā E.Coli HCP pārbaude ● Atlikušā E.Coli RNS pārbaude ● Atlikušās antibiotiku pārbaude ● Sterilitāte ● Mycoplasma ● Endotoksīns |
||
| 6 | Metodes validācija |
● specifiskums ● Precizitāte ● Precizitāte ● Linearitāte un diapazons ● Lod |
||
| 7 | Stabilitātes pētījums |
● Ilga - Termiņa stabilitāte ● Paātrināta stabilitāte ● Stresa pārbaude |
||
Priekšrocības
| Mūsu plazmīdu sistēmas priekšrocības:
• Neatkarīgi izstrādāta četras - plazmīdu sistēma ar kanamicīnu - Resistences gēns • sistēma ar ilgstošas optimizācijas spēju • Plazmīdu secības ir izsekojamas, atbilst prasībām un efektīvas • Plaša pieredze veiksmīgā Indijas iesniegšanā • Automašīna - T šūnu paraugi klīniskai lietošanai pašlaik ražo un tiek izmantoti • 2 - 5 krokas augstāki titri pēc mūsu plazmīdu sistēmas izmantošanas no salīdzināšanas vairākos projektos |
Mūsu plazmīdu ražošanas priekšrocības: • Bez antibiotikām visā ražošanas procesā • Plazmīdu ražošana un banku izveidošana atsevišķās darbnīcās • Pilnīga izolācija starp sterilām un sterilām vietām • Galaproduktu izsniegšana, izmantojot izolatoru • Pabeigtas CTD dokumentācijas iesaiņojuma plazmīdai (lentivīrusu vektoram), samazinot iesniegšanas sagatavošanas laiku par 3 - 4 mēnešiem, ar dažu produktu, kas piešķirti provizoriskam apstiprinājumam, un pašlaik I fāzē. |
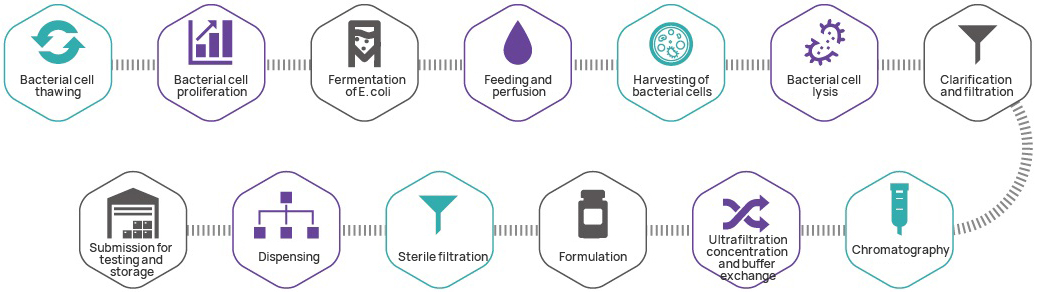
Ražošanas process
Kvalitātes kontrole
| Testa vienums | Testa metode | |
| Izskats | Vizuālā pārbaude | |
| Identifikācija | 1. identifikācija | Ierobežojuma kartēšana |
| 2. identifikācija | Sangera secība | |
| Pārbaudīt | pH | CHP 2020 0631 metode |
| Tīrība | Augstas veiktspējas šķidruma hromatogrāfija (HPLC) | |
| Atlikušais E.Coli saimnieka šūnu proteīns | Elisa | |
| Atlikušais E.Coli DNS | Q - PCR | |
| Atlikušais E.Coli RNS | Q - PCR | |
|
Atlikušās antibiotikas |
Elisa | |
| Endotoksīns | CHP 2020 Metode 1143 | |
| Sterilitāte | CHP 2020 METODE 1101 | |
| Koncentrācijas noteikšana | DNS koncentrācija | CHP 2020 metode 0401 |
Projekta laika skala
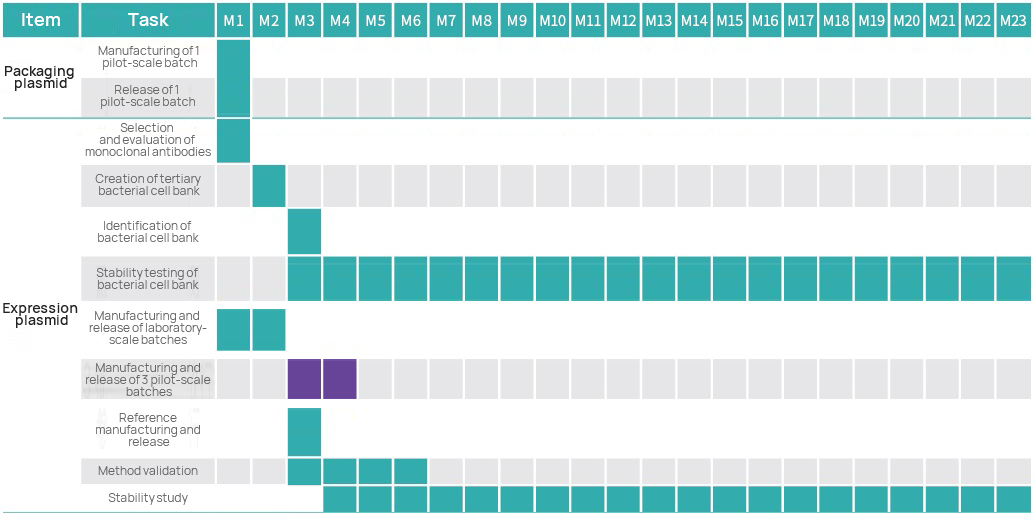
Projektu vadības plāns
Hillgene projektu vadības komanda, kas sastāv no galvenajiem zinātniekiem, projektu vadītājiem, projektu kvalitātes nodrošināšanas un GMP ekspertiem, centīsies nodrošināt katra GMP projekta vienmērīgu un pareizu darbību.