Layanan CDMO untuk plasmid - grade ind
Layanan
| Layanan CDMO untuk plasmid | ||||
| Tipe | Layanan | |||
| Kelas ind | 1 | Secara independen mengembangkan empat - sistem plasmid |
● Generasi Ketiga Empat - Sistem Plasmid ● Kanamycin - gen resistensi ● Memberikan lisensi, jika diperlukan |
● Mengikuti standar untuk diserahkan di Cina dan AS ● Lokakarya penuh - GMP ● Area terpisah untuk membuat bank sel ● Lokakarya terpisah dalam area non - steril dan steril ● Sistem manajemen kualitas GMP |
| 2 | GMP penciptaan bank sel bakteri |
● Pemilihan antibodi monoklonal ● Jumlah bank sel yang dapat disesuaikan yang akan dibuat ● Studi stabilitas bank sel |
||
| 3 | Pengembangan Metode Proses dan Uji |
● Persyaratan proyek berikut (tunduk pada perubahan yang disesuaikan) |
||
| 4 | Pembuatan plasmid GMP |
● Output produksi: 10 mg ~ 1 g (tunduk pada perubahan yang disesuaikan) ● Volume fermentasi: 3 ~ 30 L (tunduk pada perubahan yang disesuaikan) ● Metode Pemurnian: Tiga - Pendekatan Langkah/Dua - Pendekatan Langkah |
||
| 5 | Pengujian plasmid |
● Kemurnian (HPLC) ● Pengujian DNA E.Coli residual ● Tes HCP E.Coli Residual ● Tes RNA E.Coli Residual ● Pengujian antibiotik residual ● Sterilitas ● Mycoplasma ● Endotoksin |
||
| 6 | Validasi metode |
● Spesifisitas ● Akurasi ● Presisi ● Linearitas dan jangkauan ● LOD |
||
| 7 | Studi stabilitas |
● Stabilitas jangka panjang ● Stabilitas yang dipercepat ● Pengujian stres |
||
Keuntungan
| Keuntungan dari sistem plasmid kami:
• Sistem empat - plasmid yang dikembangkan secara independen dengan Kanamycin - gen resistensi • Suatu sistem dengan kemampuan optimasi berkelanjutan • Urutan plasmid dapat dilacak, sesuai dengan persyaratan, dan efisien • Pengalaman luas dalam pengajuan Ind yang sukses • CAR - Sampel sel T untuk penggunaan klinis saat ini manufaktur dan digunakan • 2 - 5 lipatan titer yang lebih tinggi setelah menggunakan sistem plasmid kami dari perbandingan dalam beberapa proyek |
Keuntungan dari manufaktur plasmid kami: • Bebas antibiotik di seluruh proses pembuatan • Produksi plasmid dan pembuatan bank dalam lokakarya terpisah • Isolasi lengkap antara area non - steril dan steril • Membagikan produk akhir menggunakan isolator • Dokumen CTD yang diselesaikan untuk pengemasan plasmid (untuk vektor lentiviral), mengurangi waktu persiapan pengiriman dengan 3 - 4 bulan, dengan beberapa produk diberikan persetujuan awal dan saat ini dalam fase I studi klinis |
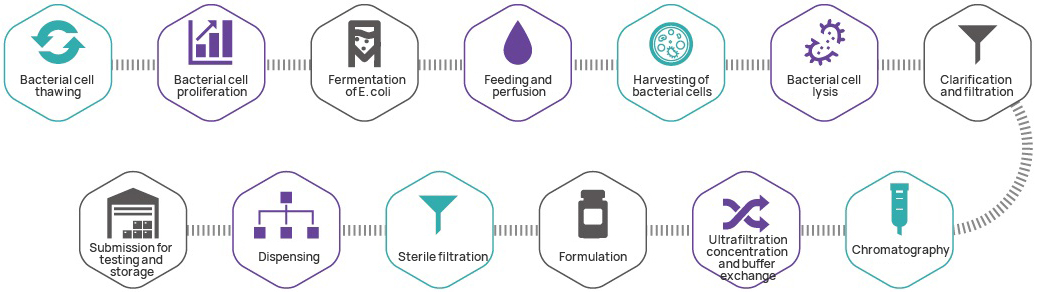
Proses pembuatan
Kontrol kualitas
| Item tes | Metode pengujian | |
| Penampilan | Inspeksi Visual | |
| Identifikasi | Identifikasi 1 | Pemetaan Pembatasan |
| Identifikasi 2 | Sequencing Sanger | |
| Tes | pH | Metode 0631 dari CHP 2020 |
| Kemurnian | Kromatografi cair kinerja tinggi (HPLC) | |
| Protein sel inang E.Coli residual | Elisa | |
| Residual E.Coli DNA | Q - PCR | |
| Residual e.coli RNA | Q - PCR | |
|
Antibiotik residual |
Elisa | |
| Endotoksin | Metode 1143 dari CHP 2020 | |
| Kemandulan | Metode 1101 dari CHP 2020 | |
| Penentuan konsentrasi | Konsentrasi DNA | Metode 0401 dari CHP 2020 |
Garis Waktu Proyek
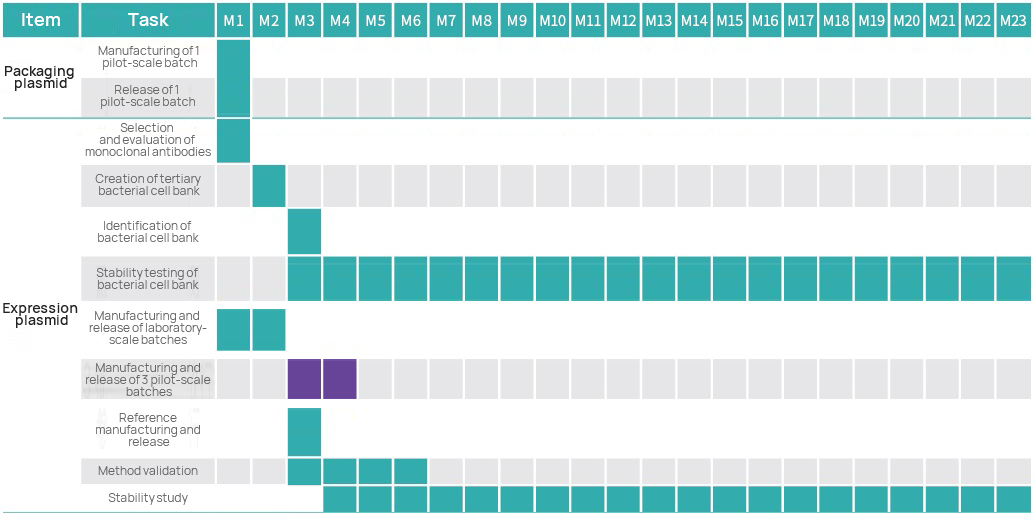
Rencana Manajemen Proyek
Tim Manajemen Proyek Hillgene, yang terdiri dari Kepala Ilmuwan, Manajer Proyek, Pakar Proyek QA dan GMP, akan melakukan upaya untuk memastikan pengoperasian yang lancar dan baik dari masing -masing dan setiap proyek GMP.