La necessitat de les proves d’ADN residual de E.coli
En camps com la teràpia cel·lular i gènica, els plasmids virals s’amplifiquen i es fermen amb E. coli com a hoste. El plasmidi amplificat ha de sotmetre’s a un control de qualitat de l’ADN residual de E.Coli abans que es pugui utilitzar per infectar 293 cèl·lules i empaquetar el virus. Per tant, la detecció de l’ADN residual de E.coli és fonamental.
Requisits reguladors i mètodes de prova
Les directrius actuals de l’OMS i dels EUA de la FDA recomanen que l’ADN residual en productes acabats no sigui superior a 10 ng/agent, i la FDA dels Estats Units també afirma que l’ADN residual en cèl·lules hostes de biològics no hauria de ser superior a 100 pg/agent. Els principis generals de la farmacopea europea estipulen que el límit de l’ADN residual en productes biològics no ha de ser superior a 10 ng/dosi, però el límit d’ADN residual per a algunes vacunes particulars és més estricta, per exemple, l’ADN residual en la vacuna inactivada contra l’hepatitis A no ha de ser superior a 100 pg/dosis, i en la vacuna contra la vacuna contra hepatitis no ha de ser superior a la vacuna contra hepatitis. PG/dosi. L’edició del 2020 de la farmacopea xinesa, la part III, estipula que el residu d’ADN en preparacions biològiques produïdes en una matriu cel·lular no hauria de superar els 100 pg/dosi, i el residu d’ADN en vacunes produïdes en una matriu bacteriana o de fong no hauria de superar els 10 ng/dosi.
A més, per als mètodes de determinació de residus d’ADN exògens, les farmacopea nacionals també donen recomanacions d’orientació. L’edició dels EUA de la Farmacopea 2017 de l’USP40 - NF35 Disposició general 1130 descriu tres mètodes per a la determinació de residus d’ADN exògens, que són la hibridació de sonda d’ADN, el mètode llindar i el mètode de PCR real de temps real. La Farmacopea Europea proposa PCR quantitativa de temps i mètode immunoenzimàtic, dos mètodes analítics sensibles per quantificar l'ADN residual de cèl·lules hostes. La versió xinesa Pharmacopeia 2020 de les tres regles generals 3407 també estipula que els mètodes de detecció de residus d’ADN de cèl·lules hostes són la hibridació de la sonda d’ADN, la tinció de fluorescència i la PCR quantitativa.
Entre ells, el mètode QPCR té una sensibilitat extremadament alta, l’especificitat i la precisió de la seqüència, que poden proporcionar un mitjà de detecció fiable per a la indústria biofarmacèutica en la investigació de processos i el control de qualitat dels productes acabats, i ara s’ha convertit en el mètode de detecció preferit per a cada fabricant de biològics.
Informació sobre els productes Bluekit
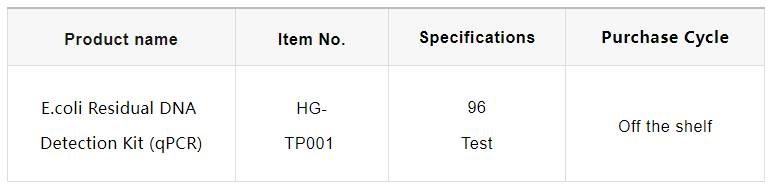
Característiques del producte
Detecció ràpida, forta especificitat, rendiment fiable, el límit de detecció més baix pot arribar al nivell de “FG”.
Paràmetres del producte
- Interval de detecció: 3.00 × 101 ~ 3,00 × 105fg/μl
- Límit de quantificació :00 × 101fg/μl
- Límit de detecció :00 FG/μL
- Precisió: CV% ≤ 15%.
Problemes i precaucions de detecció comunes
1. Aquest kit és per a ús de la investigació in vitro, no per al diagnòstic clínic.
2. El kit s’ha d’utilitzar dins del període de validesa.
3. Es recomana fondre tots els components del kit en un entorn de baixa temperatura i després.
4. Només compleix estrictament les instruccions del mètode d’operació, tot l’ús del kit que recolza els reactius per assegurar el millor efecte de detecció.
5. Fixeu -vos en els diferents passos de mostreig de manera puntual per substituir la punta, per evitar la contaminació creuada, evitar obrir la tapa durant molt de temps.
6. Els resultats de la prova final es poden veure afectats significativament per l'efectivitat dels reactius, els mètodes de funcionament de l'operador i l'entorn de prova.
Consulta de productes
Telèfon: +86 - 18013115357
Correu electrònic:info@hillgene.com
Hora del missatge: 2024 - 01 - 11 10:31:30