Mga Serbisyo ng CDMO para sa Lentiviral Vectors - Klinikal na grado
Mga Serbisyo
| CDMO Services para sa mga lentiviral vectors (Hilenti®Platform) | ||||
| Mga uri | Mga Serbisyo | |||
| Klinikal na grado | 1 | Ang paggawa ng GMP ng mga lentiviral vectors |
● Proseso ng Bioreactor: 5 ~ 50 L Pagtatapon ng Proseso ng Bioreactor (napapailalim sa mga na -customize na pagbabago) ● Scale ng Produksyon: 2 ~ 30 L (napapailalim sa mga pasadyang pagbabago) |
● Buong - GMP Workshop ● Paghiwalayin ang mga workshop sa loob ng hindi - sterile at sterile na mga lugar ● Sistema ng pamamahala ng kalidad ng GMP ● Napatunayan na halaman, pasilidad at kagamitan na sumusunod sa mga kinakailangan sa klinikal |
| 2 | Paglipat ng Teknolohiya |
● Paglipat ng teknolohiya ● Pagtanggap ng paglipat ng teknolohiya |
● Well - Itinatag na Plano para sa Paglipat ng Teknolohiya ● Well - itinatag na plano para sa pagtanggap ng paglipat ng teknolohiya ● Plano para sa paglilipat ng iba't ibang mga teknolohiya sa iba't ibang mga phase |
|
Kalamangan
| Mga kalamangan ng paggamit ng aming platform para sa suwero - libreng suspensyon na kultura ng mga lentiviral vectors:
• Libre ng Mga Hayop - nagmula sa mga sangkap sa buong proseso • Linearly scaled up production of lentiviral vectors • Paggamit ng isang solong lalagyan ng isang 50 L disposable bioreactor • Paglikha ng Cell Bank sa magkakahiwalay na mga workshop • Dispensing panghuling produkto gamit ang isang sterile isolator • Nakatuon na sistema ng lentivirus para sa mga cell ng kotse - t, na may mataas na kahusayan sa impeksyon • Mababang gastos sa produksyon at mga gastos sa pagsubok (walang mga kinakailangan sa pagsubok para sa BSA at natitirang pancreatic enzymes) • Maraming matagumpay na pagsumite ng IND sa NMPA ng mga lentiviral vectors para sa CAR - T cells |
Proseso ng Paggawa

KONTROL CONTROL
| Produkto | Pagsubok ng item | Paraan ng Pagsubok |
| Pag -aani ng likido | Adventitious kontaminasyon ng virus | Paraan 3302 ng CHP 2020 |
| Pagtitiklop - karampatang lentiviruses | Pamamaraan ng Cell Culture Culture | |
| Substance ng Gamot/Tapos na Produkto | Hitsura | Visual inspeksyon |
| Sterility | Paraan 1101 ng CHP 2020 | |
| Mycoplasma |
Paraan 3301 ng CHP 2020 |
|
| pH | Paraan 0631 ng CHP 2020 | |
| Osmolality | Paraan 0632 ng CHP 2020 | |
| Target na pagkakakilanlan ng istraktura ng gene | Pagkakasunud -sunod | |
| Residual host cell protein | Elisa | |
| Physical Titer (P24) | Elisa | |
| Functional titer | Daloy ng cytometry | |
| Endotoxin | Paraan 1143 ng CHP 2020 | |
| Residual Benzonase | Elisa | |
| Residual host cell DNA | q - pcr | |
| Residual E1A Gene Transfer | CO - Paraan ng Kultura | |
| Residual SV40 Gene Transfer | CO - Paraan ng Kultura |
Timeline ng proyekto
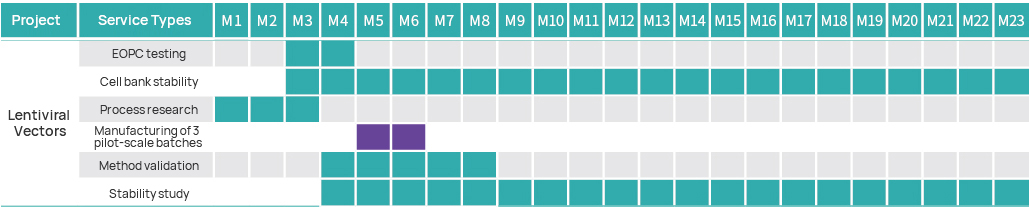
Plano ng Pamamahala ng Proyekto
Ang koponan ng pamamahala ng proyekto ng Hillgene, na binubuo ng mga punong siyentipiko, tagapamahala ng proyekto, mga eksperto sa proyekto ng QA at GMP, ay magsisikap upang matiyak ang maayos at maayos na operasyon ng bawat proyekto ng GMP.